Es hat schon etwas Philosophisches, wenn man über den Aufbau unserer Welt nachdenkt. Woraus besteht Materie eigentlich? Wie ist es möglich, dass aus winzigen, unsichtbaren Teilchen die ganze Vielfalt unserer stofflichen Welt entsteht? Genau mit diesen Fragen beschäftigt sich die Atomphysik.
Atome sind die Grundbausteine aller Elemente. Sie bestehen aus einem Atomkern und einer Elektronenhülle und ihr Aufbau entscheidet darüber, wie Stoffe sich verhalten. Die Atomphysik untersucht dabei vor allem die Struktur der Atome, die Verteilung der Elektronen und ihre Wechselwirkungen. Die Erforschung des Atomkerns gehört dagegen heute meist zur Kernphysik und nicht mehr zur Atomphysik im engeren Sinn.
Wenn dich also interessiert, wie Atome aufgebaut sind und warum die Quantenmechanik dabei eine so wichtige Rolle spielt, dann steig mit uns ein in die Welt der Atomphysik.

Was ist ein Atom? Aufbau und Eigenschaften
Atome sind die Grundbausteine der Materie. Alle Stoffe, die wir kennen – von Luft und Wasser bis zu Metallen oder Gesteinen – bestehen letztlich aus Atomen. Insgesamt gibt es in der Natur rund 92 verschiedene Elemente, deren Atome sich in Aufbau und Eigenschaften unterscheiden.1
Aufbau eines Atoms
Ein Atom besteht aus zwei grundlegenden Bereichen:
- Atomkern: befindet sich im Zentrum des Atoms und enthält fast seine gesamte Masse
- Elektronenhülle: umgibt den Kern und enthält die negativ geladenen Elektronen
Der Atomkern setzt sich aus positiv geladenen Protonen und elektrisch neutralen Neutronen zusammen. Zusammen werden diese Teilchen als Nukleonen bezeichnet.
In der Atomphysik spielen mehrere grundlegende Teilchen eine wichtige Rolle. Einige bilden den Aufbau der Atome, andere erklären wichtige physikalische Phänomene.
⚛️ Proton
Positiv geladenes Teilchen im Atomkern. Die Anzahl der Protonen bestimmt, um welches chemische Element es sich handelt (Ordnungszahl).
⚪ Neutron
Elektrisch neutrales Teilchen im Atomkern. Neutronen tragen zur Masse des Atoms bei und beeinflussen die Stabilität des Kerns.
⚡ Elektron
Negativ geladenes Teilchen in der Elektronenhülle. Elektronen bestimmen, wie Atome miteinander reagieren und chemische Bindungen bilden.
In der Elektronenhülle bewegen sich die negativ geladenen Elektronen. Obwohl sie nur einen sehr kleinen Teil zur Gesamtmasse beitragen, bestimmen sie maßgeblich die chemischen Eigenschaften eines Atoms und damit auch, wie Atome miteinander reagieren und Moleküle bilden.
Bei Superprof findest du Physik Nachhilfe Bonn!
Die Entdeckung des Atomkerns
Wie klein und zugleich erstaunlich strukturiert ein Atom ist, zeigte ein berühmtes Experiment des Physikers Ernest Rutherford zu Beginn des 20. Jahrhunderts. In seinem Streuversuch beschoss er eine dünne Goldfolie mit sogenannten α-Teilchen (Heliumkernen).
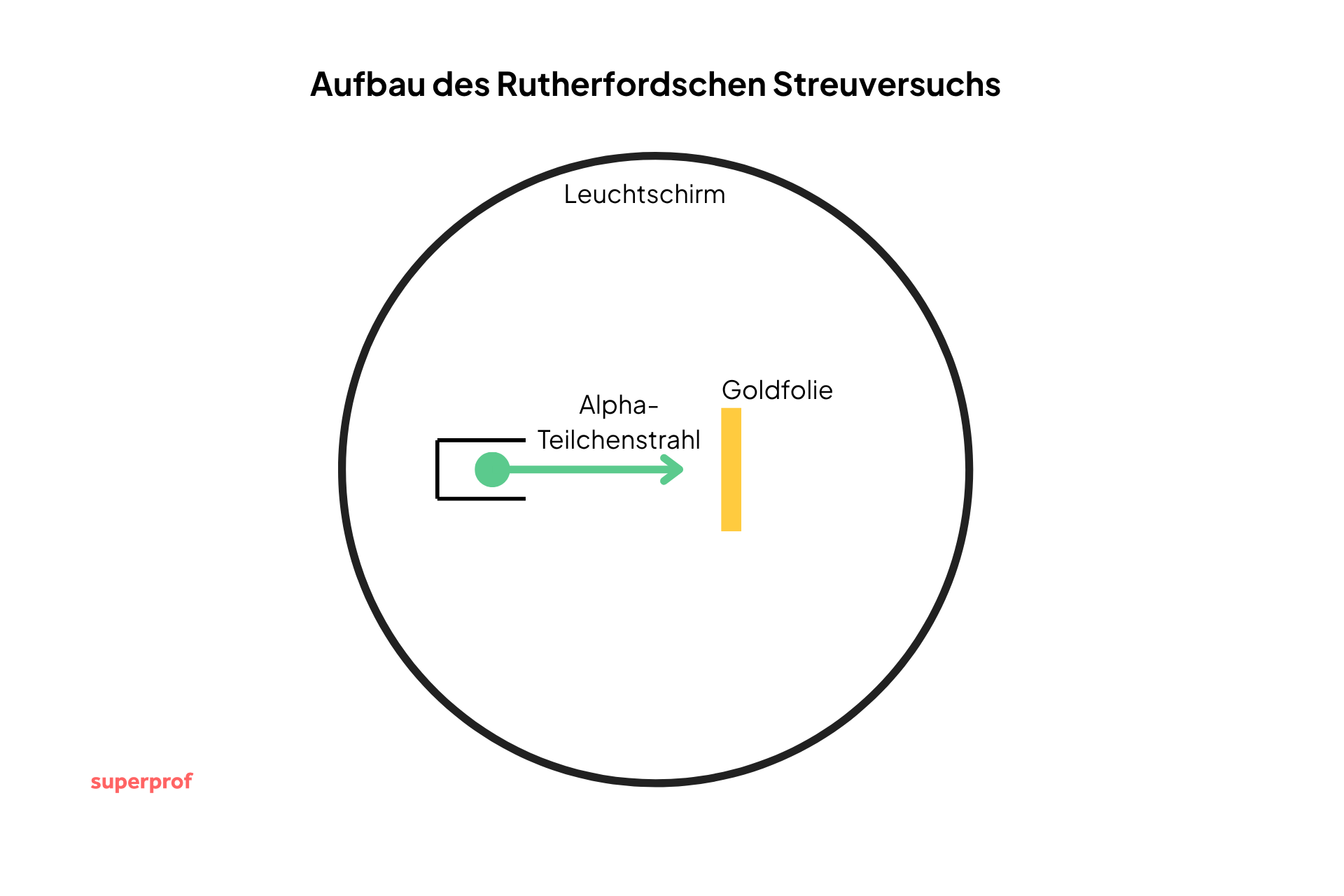
Dabei machte er zwei wichtige Beobachtungen:
- Die meisten α-Teilchen durchdrangen die Goldfolie ohne Ablenkung.
- Einige wenige wurden stark abgelenkt oder sogar zurückgestreut.
Daraus zog Rutherford einen entscheidenden Schluss: Die gesamte Masse des Atoms muss in einem sehr kleinen, positiv geladenen Atomkern konzentriert sein. Die Elektronen befinden sich dagegen in einer viel größeren Hülle um diesen Kern. Ein Atom besteht also größtenteils aus leerem Raum.
Wir erklären dir übrigens auch die Wärmelehre!
Historische Entwicklung der Atommodelle
Unser heutiges Verständnis vom Aufbau der Atome entstand nicht über Nacht. Vielmehr entwickelte sich das Bild des Atoms Schritt für Schritt über viele Jahrhunderte hinweg – von ersten philosophischen Ideen bis zu den präzisen Modellen der modernen Physik.
Frühe Atommodelle und ihre Grenzen

Der Gedanke, dass Materie aus winzigen Teilchen zusammengesetzt ist, hat eine lange Geschichte. Schon um 400 v. Chr. brachte der griechische Philosoph Demokrit den Begriff Atomon auf, was so viel wie "etwas Unteilbares" bedeutet.2
Seinem Glauben nach bestand die Welt aus Atomen und leerem Raum. Diese Idee wurde jedoch über lange Zeit vergessen. Für viele Jahrhunderte war die aristotelische Lehre von den vier Elementen Feuer, Wasser, Luft und Erde die vorherrschende Ansicht.
Im 19. Jahrhundert nahm der englische Naturforscher John Dalton diese Idee wieder auf. In seinem Atommodell von 1808 stellte er Atome als die kleinsten, unteilbaren Bausteine der Materie dar.
Jedes chemische Element besteht aus identischen Atomen, die sich in Masse und Größe von den Atomen anderer Elemente unterscheiden. Obwohl sich später herausstellte, dass Atome doch teilbar sind, war Daltons Theorie ein bedeutender Fortschritt für die moderne Naturwissenschaft.
Im Jahr 1903 entwarf Joseph John Thomson ein weiteres Atommodell. Sein Rosinenkuchenmodell stellte das Atom als eine positiv geladene Kugel dar, in die negativ geladene Elektronen eingebettet waren, ähnlich wie Rosinen in einem Kuchen.
Ernest Rutherford war letztlich derjenige, der den entscheidenden Durchbruch erzielte. In seinem bekannten Goldfolienexperiment ließ er α-Teilchen auf eine dünne Goldfolie treffen. Während die meisten Teilchen die Folie ohne Ablenkung passierten, wurden einige wenige stark zurückgestreut.
Rutherford schloss daraus, dass die Masse eines Atoms in einem winzigen, positiv geladenen Kern konzentriert sein muss, während die Elektronen eine große Hülle um diesen Kern bilden.
Übrigens, für Physiker*innen offensichtlich, für Laien nicht: Quantenmechanik ist nicht dasselbe wie die klassische Mechanik!
Das Bohr'sche Atommodell und seine Bedeutung
Niels Bohr schaffte im Jahr 1913 eine bedeutende Weiterentwicklung des Kernmodells. Er brachte die Entdeckungen Rutherfords mit den damals aktuellen Konzepten der Quantenphysik zusammen, die von Forschern wie Max Planck und Albert Einstein ausgearbeitet wurden.
Nach dem Bohrschen Atommodell umkreisen Elektronen den Atomkern nicht beliebig, sondern befinden sich auf festgelegten Bahnen, den sogenannten Energieniveaus. Indem sie Energie aufnehmen oder abgeben, können Elektronen zwischen diesen Bahnen wechseln. Dieser Übergang ist der Grund für die Linienspektren von Atomen – die einzigartigen Lichtlinien, die jedes Element aussendet.
⚛️ Warum fallen Elektronen nicht in den Atomkern?
Nach den Gesetzen der klassischen Physik müssten Elektronen ständig Energie verlieren und schließlich in den Atomkern stürzen. In Wirklichkeit passiert das aber nicht.
Die Quantenmechanik erklärt die Stabilität von Atomen durch mehrere Prinzipien:
🌌 Elektronen können sich nur auf bestimmten Energieniveaus befinden.
⚡ Ein Elektron kann nicht einfach beliebige Energie verlieren.
🧠 Das Pauli-Prinzip verhindert, dass Elektronen denselben Quantenzustand einnehmen.
🔬 Dadurch bleibt die Elektronenhülle stabil.
Obwohl das Modell erfolgreich war, hatte es auch Einschränkungen. Die klassischen Elektrodynamikgesetze besagen, dass beschleunigte Elektronen ständig Energie verlieren und letztlich in den Kern fallen müssten. Die Stabilität des Atoms konnte das Bohrsche Modell nur durch zusätzliche Annahmen erklären, und es war nur eingeschränkt auf komplexere Atome anwendbar.
Interessierst du dich auch für die Optik?
Vom Orbitalmodell zur Quantenmechanik
Der entscheidende Fortschritt kam in den 1920er-Jahren mit der Entwicklung der Quantenmechanik. Physiker wie Erwin Schrödinger, Werner Heisenberg, Louis de Broglie und Max Born entwickelten eine völlig neue Beschreibung der atomaren Welt.
Damit wurde das Bohrsche Atommodell grundlegend erweitert. Elektronen wurden nun nicht mehr als Teilchen auf festen Bahnen verstanden, sondern mit Hilfe quantenmechanischer Modelle beschrieben. Diese neue Sichtweise führte schließlich zum modernen Orbitalmodell, auf das wir im nächsten Kapitel genauer eingehen.
Auch Werner Heisenberg trug entscheidend zum neuen Verständnis der Atomstruktur bei. Mit seiner Unschärferelation zeigte er, dass Ort und Geschwindigkeit eines Elektrons nicht gleichzeitig exakt bestimmt werden können. Damit wurde klar: Auf der atomaren Ebene gelten andere physikalische Regeln als in unserer alltäglichen Welt.

Grundlagen der Quantenmechanik in der Atomphysik
Mit der Entwicklung der Quantenmechanik begann im frühen 20. Jahrhundert ein völlig neues Kapitel der Physik. Viele Beobachtungen ließen sich mit den Gesetzen der klassischen Physik nicht mehr erklären. Erst durch neue Modelle und Experimente wurde verständlich, wie sich Elektronen und Licht auf atomarer Ebene tatsächlich verhalten.
Interessieren dich auch weitere Teilgebiete der Physik?
Wellen-Teilchen-Dualismus und der Photoeffekt
Einen wichtigen Meilenstein lieferte Albert Einstein im Jahr 1905 mit seiner Erklärung des Photoeffekts (auch lichtelektrischer Effekt genannt). In einem Experiment wurde eine negativ geladene Metallplatte mit Licht bestrahlt. Man stellte dabei fest, dass Licht Elektronen aus dem Metall herauslösen kann.
Dabei machte man zwei entscheidende Beobachtungen:
- Wird die Intensität des Lichts erhöht, werden mehr Elektronen freigesetzt.
- Wird jedoch die Frequenz des Lichts zu niedrig, treten überhaupt keine Elektronen mehr aus – selbst bei sehr hoher Intensität.
Diese Erkenntnis stand im Widerspruch zur klassischen Auffassung von Licht als einer reinen Welle. Aus diesem Grund erklärte Einstein das Phänomen mit einer neuen Idee: Licht setzt sich aus winzigen Energieeinheiten zusammen, die man Photonen nennt. Wenn ein Photon ein Elektron trifft, kann es seine Energie an das Elektron übertragen und es somit aus dem Metall lösen.
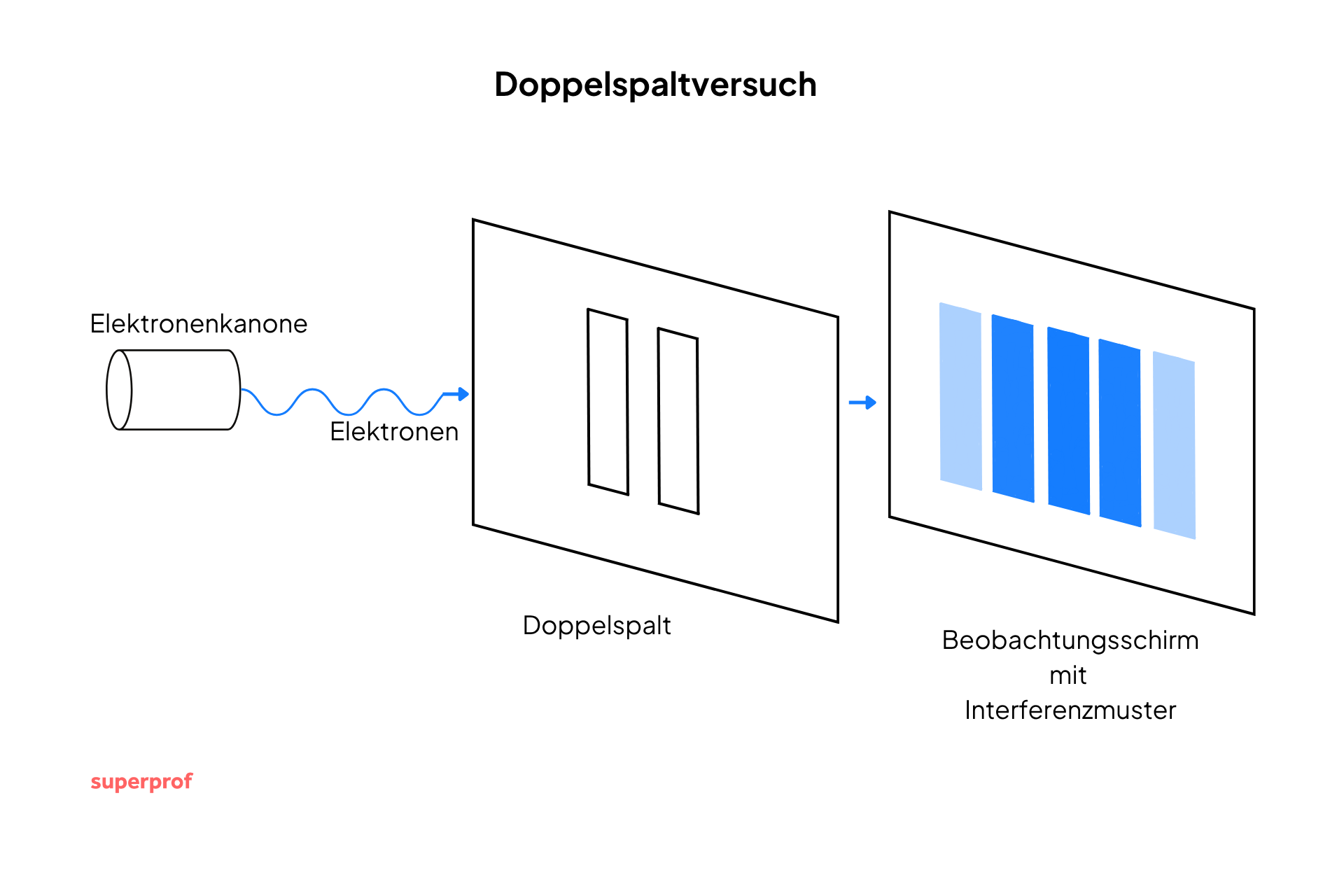
Ein weiteres bekanntes Experiment ist der Doppelspaltversuch. Hierbei werden Teilchen wie Elektronen durch zwei enge Spalte auf einen Schirm geschossen. Man hätte zwei Streifen auf dem Schirm erwarten sollen, doch tatsächlich entsteht ein Interferenzmuster, wie es sonst nur von Wellen bekannt ist.
Dieses Experiment illustrierte, dass Teilchen sich unter bestimmten Umständen wie Wellen verhalten können.
Wellenfunktionen und das Pauli-Prinzip
Die berühmte Schrödinger-Gleichung ermöglichte es zum ersten Mal, die möglichen Zustände eines Elektrons im Atom mathematisch zu erfassen.
Dabei wurde deutlich, dass Elektronen nicht auf festen Bahnen um den Kern kreisen. Die sogenannte Wellenfunktion beschreibt vielmehr die Wahrscheinlichkeit, ein Elektron in einem bestimmten Bereich des Atoms zu finden.
Diese Bereiche nennt man Orbitale. Sie lassen sich als eine Art Elektronenwolke verstehen: also als Raumzonen, in denen sich ein Elektron mit bestimmter Wahrscheinlichkeit aufhält. Damit ersetzte das Orbitalmodell die ältere Vorstellung von klaren Elektronenbahnen.
Auch Wolfgang Pauli hat einen bedeutenden Beitrag geleistet. Nach seinem Pauli-Prinzip ist es unmöglich, dass zwei Elektronen in einem Atom denselben Quantenzustand einnehmen. Dieses Prinzip ist von großer Bedeutung für die Struktur der Elektronenhüllen und erklärt zahlreiche Eigenschaften der Elemente.
Das Periodensystem und Elektronenkonfigurationen
Das Periodensystem der Elemente wurde bereits im 19. Jahrhundert von Dmitri Mendelejew und Lothar Meyer entwickelt. Sie ordneten die bekannten Elemente nach ihren chemischen Eigenschaften und entdeckten dabei regelmäßige Muster.
Erst mit Hilfe der Quantenmechanik konnte man später erklären, warum diese Ordnung funktioniert. Die chemischen Eigenschaften eines Elements hängen vor allem von der Elektronenstruktur seiner Atome ab.
Die wichtigsten Zusammenhänge sind:
- Die Ordnungszahl bestimmt die Anzahl der Protonen im Kern und damit auch die Anzahl der Elektronen.
- Elektronen besetzen bestimmte Orbitale und Energieniveaus.
- Elemente mit ähnlicher Elektronenstruktur besitzen ähnliche chemische Eigenschaften.
So erklärt die Atomphysik, warum Elemente im Periodensystem in bestimmten Gruppen stehen und sich chemisch ähnlich verhalten.
Brauchst du Physik Nachhilfe in Hamburg?
Anwendungen der Atomphysik
Die Atomphysik ist nicht nur ein theoretisches Forschungsgebiet. Viele ihrer Erkenntnisse haben zu Technologien geführt, die heute in Wissenschaft, Medizin und Technik eine wichtige Rolle spielen. Methoden, die ursprünglich für atomphysikalische Experimente entwickelt wurden, finden inzwischen in vielen Bereichen praktische Anwendungen.
Lasertechnologie und Spektroskopie
Im 19. Jahrhundert machten Gustav Kirchhoff und Robert Bunsen einen bedeutenden Fortschritt, indem sie mit der Spektralanalyse die Möglichkeit entdeckten, die chemische Zusammensetzung von Sternen zu bestimmen.
Sie analysierten das Sonnenlicht und entdeckten, dass die Spektrallinien von Elementen stammen, die auch auf der Erde zu finden sind. Erstmals wurde damit experimentell bewiesen, dass die gleichen Elemente im Universum vorkommen wie auf unserem Planeten.
Die Analyse von Spektrallinien bleibt bis heute ein bedeutendes Instrument der Atomphysik. Eine große Anzahl moderner Analyseverfahren, wie sie beispielsweise in der chemischen Analytik, der Materialwissenschaft oder der Astrophysik Anwendung findet, hat sich daraus entwickelt.

Auch der Laser ist eine direkte Anwendung atomphysikalischer Prinzipien. Laserstrahlen werden heute in vielen Bereichen eingesetzt, zum Beispiel:
- 🔬 in der Forschung und Messtechnik
- 💿 bei Datenspeicherung und Kommunikationstechnologie
- 🏥 in der Medizin, etwa bei Operationen oder Augenbehandlungen
- 📏 bei präzisen Messungen von Entfernungen und Frequenzen
Atomuhren und Zeitmessung
Eine besonders faszinierende Anwendung der Atomphysik sind Atomuhren. Sie nutzen die extrem präzisen Energieniveaus von Atomen, um Zeit zu messen.
In einer Atomuhr wird die Frequenz elektromagnetischer Strahlung gemessen, die entsteht, wenn Elektronen zwischen bestimmten Energieniveaus wechseln. Diese Frequenz ist so konstant, dass Atomuhren heute zu den genauesten Messinstrumenten der Welt gehören.
Atomuhren sind unter anderem wichtig für:
- 🌍 Satellitennavigation (GPS)
- 🛰️ Raumfahrt und Satellitentechnik
- 📡 Telekommunikation
- ⏱️ internationale Zeitstandards
Ohne Atomuhren würden viele moderne Navigations- und Kommunikationssysteme nicht funktionieren.
Bei Problemen ist Physik Nachhilfe immer eine gute Idee.
Medizinische Bildgebung und Diagnostik
Selbst in der Medizin ist die Atomphysik von großer Bedeutung. Ein frühes Beispiel ist die Röntgenstrahlung, die Wilhelm Conrad Röntgen 1895 entdeckte.3 Röntgenstrahlen sind in der Lage, das Innere des Körpers sichtbar zu machen, und sie zählen bis heute zu den bedeutendsten Diagnoseverfahren.
Zudem beruhen zahlreiche moderne Verfahren auf den Grundlagen der Atomphysik. Ein bekanntes Beispiel ist die Kernspinresonanz, welche in der Medizin als Magnetresonanztomographie (MRT) genutzt wird. Diese Methode erlaubt es, Bilder von Organen und Gewebe in hoher Detailgenauigkeit zu erstellen.
Zukunftsperspektiven der Atomphysik
Trotz ihrer langen Geschichte ist die Atomphysik alles andere als eine abgeschlossene Wissenschaft. Über die letzten Jahrzehnte hinweg sind viele neue Ansätze entstanden, um einzelne Atome zu untersuchen und sogar gezielt zu manipulieren.
Eine bedeutende Entwicklung ist die sogenannte Laserkühlung. Durch den Einsatz von Laserstrahlen ist es möglich, Atome stark abzubremsen und sie auf Temperaturen nahe dem absoluten Nullpunkt zu bringen. So entstehen neuartige Materiezustände wie das Bose-Einstein-Kondensat, in dem viele Atome gleichzeitig quantenmechanische Eigenschaften zeigen.
Atomphysikalische Effekte kommen ebenfalls in der Quantenkryptographie zum Einsatz. Informationen können theoretisch vollkommen abhörsicher über verschränkte Zustände übertragen werden.
Außerdem sind Wissenschaftlerinnen und Wissenschaftler dabei, die gezielte Kontrolle und Manipulation von einzelnen Atomen zu erforschen. Mit Hilfe von Ionenfallen ist es möglich, ionisierte Atome über längere Zeiträume zu speichern und sie mit hoher Genauigkeit zu untersuchen.
Wie wäre es mit Physik Nachhilfe online?
Referenzen
- Mainz, J. G. (n.d.). Die Welt um Elemente erweitert | Institut für Kernchemie. Johannes Gutenberg-Universität Mainz. https://www.kernchemie.uni-mainz.de/die-welt-um-elemente-erweitert/
- Löbl, R. (1987). Demokrits atomphysik.
- Otto Glasser: Wilhelm Conrad Röntgen und die Geschichte der Röntgenstrahlen. 2. Auflage. Springer, Berlin 1959.
Mit KI zusammenfassen:















