Wusstest du, dass dir täglich Basen begegnen? Beim Händewaschen mit Seife, beim Putzen oder beim Backen mit Natron. Hinter all diesen Beispielen steckt ein gemeinsames Prinzip: Eine Base ist eine chemische Verbindung, die in wässriger Lösung Hydroxidionen (OH⁻) freisetzt und somit den pH-Wert erhöht. Sie fungiert als Protonenakzeptor und kann Säuren neutralisieren.
Genau deshalb sind Basen in der Chemie so wichtig: Sie sind der „Gegenspieler“ der Säuren und spielen eine zentrale Rolle in Säure-Base-Reaktionen, im Labor und in vielen Anwendungen im Alltag und in der Industrie.

Was ist eine Base?
Im Alltag fallen Basen oft durch typische Eigenschaften auf. Viele basische Lösungen fühlen sich seifig oder glatt an. Das ist ein Effekt, der entsteht, weil Basen Fette auf der Haut leicht angreifen und dabei seifenähnliche Stoffe bilden. Außerdem schmecken viele Basen bitter. Trotzdem gilt natürlich ganz klar: Chemikalien dürfen niemals probiert werden!
Wichtig ist auch: „Basisch“ bedeutet nicht „harmlos“. Genau wie Säuren können starke oder konzentrierte Basen ätzend wirken und Haut oder Augen schädigen.

Basen sehen zudem nicht immer gleich aus. Manche sind fest (z. B. Natriumhydroxid in Form von Pellets), andere flüssig (Natronlauge) oder sogar gasförmig, wie Ammoniak (NH₃).
Entscheidend ist nicht der Aggregatzustand, sondern ihr chemisches Verhalten.
Die wichtigste Definition (Brønsted)
Nach dem heute am häufigsten verwendeten Konzept von Brønsted ist eine Base ein Protonenakzeptor.1 Das bedeutet: Sie kann ein Proton (H⁺) aufnehmen.
Nimmt eine Base ein Proton auf, entsteht ihre sogenannte korrespondierende Säure. Beide zusammen bilden ein Säure-Base-Paar. Ein klassisches Beispiel ist die Reaktion von Ammoniak mit Wasser:
NH₃ + H₂O ⇌ NH₄⁺ + OH⁻
Hier nimmt Ammoniak (NH₃) ein Proton von Wasser auf und wird zu Ammonium (NH₄⁺). Gleichzeitig entsteht ein Hydroxidion (OH⁻), das die Lösung basisch macht.
pH-Wert als Messgröße
Ob eine Lösung basisch ist, erkennt man am pH-Wert. Liegt er über 7, spricht man von einer basischen Lösung. Der Grund: In solchen Lösungen ist die Konzentration der Hydroxidionen (OH⁻) höher als die der Oxoniumionen (H₃O⁺).
Je mehr OH⁻-Ionen vorhanden sind, desto stärker verschiebt sich das Gleichgewicht und desto höher steigt der pH-Wert. Man kann auch vom sogenannten pOH-Wert sprechen, der die OH⁻-Konzentration beschreibt, doch im Schulalltag arbeitet man meist direkt mit dem pH-Wert.
Definition und Konzepte von Basen
Der Begriff „Base“ wurde im Laufe der Chemiegeschichte immer weiterentwickelt. Je nachdem, welche Reaktionen man betrachtet, eignen sich unterschiedliche Modelle, um Basen zu beschreiben. Diese Konzepte widersprechen sich nicht, sondern beleuchten verschiedene Aspekte desselben chemischen Verhaltens.
Im Schulunterricht und in der allgemeinen Chemie hat sich vor allem das Brønsted-Konzept als wichtigste und am häufigsten verwendete Definition durchgesetzt. Es erklärt sehr anschaulich, warum Basen mit Säuren reagieren und wie Neutralisation funktioniert. Daneben gibt es jedoch weitere Modelle, die je nach Kontext hilfreich sind.
Arrhenius-Definition
Eine der ältesten Definitionen stammt von Svante Arrhenius. Nach ihm ist eine Base eine Substanz, die in Wasser Hydroxidionen (OH⁻) bildet.
Ein typisches Beispiel ist Natriumhydroxid (NaOH). Gibt man es in Wasser, zerfällt es in Natriumionen (Na⁺) und Hydroxidionen (OH⁻):
NaOH → Na⁺ + OH⁻
Die frei beweglichen OH⁻-Ionen sind verantwortlich für den basischen Charakter der Lösung und den erhöhten pH-Wert.
Die Arrhenius-Definition ist besonders anschaulich und eignet sich gut für viele Schulbeispiele. Ihr Nachteil: Sie gilt nur für Reaktionen in Wasser und erklärt nicht alle basischen Reaktionen.
Basen, die erst mit Wasser reagieren
Nicht jede Base enthält bereits ein OH⁻-Ion in ihrer Struktur. Manche Stoffe bilden Hydroxidionen erst durch Reaktion mit Wasser.
Ein wichtiges Beispiel ist Ammoniak (NH₃). Es enthält kein OH⁻, reagiert aber mit Wasser so, dass ein Hydroxidion entsteht:
NH₃ + H₂O ⇌ NH₄⁺ + OH⁻
Hier zeigt sich: Entscheidend ist nicht, ob OH⁻ schon „im Molekül steckt“, sondern ob es in Lösung gebildet wird.
Lewis-Definition
Noch allgemeiner ist die Definition nach Lewis. Danach ist eine Base ein Elektronenpaardonator. Das bedeutet, sie stellt ein freies Elektronenpaar zur Verfügung, um eine Bindung einzugehen.2
So kann Ammoniak (NH₃) mit Bortrifluorid (BF₃) reagieren:
NH₃ + BF₃ → F₃B←NH₃
Hier spendet Ammoniak ein Elektronenpaar an das Bor-Atom. Es findet keine Protonenübertragung statt und trotzdem spricht man von einer Säure-Base-Reaktion.
Die Lewis-Definition ist besonders nützlich in der organischen Chemie und in der Komplexchemie.

Eigenschaften von Basen
Basen erkennt man nicht nur am pH, sondern auch an typischen Reaktionen. Ihr chemisches Verhalten zeigt sich besonders deutlich im Kontakt mit Säuren, Indikatoren oder organischem Material wie Fetten.
Neutralisation
Eine der wichtigsten Eigenschaften von Basen ist ihre Fähigkeit zur Neutralisation. Treffen eine Base und eine Säure in passenden Mengen aufeinander, heben sich ihre Wirkungen gegenseitig auf. Dabei entsteht Wasser und ein Salz:
Base + Säure → Salz + Wasser

Ein klassisches Beispiel ist die Reaktion von Natriumhydroxid mit Salzsäure:
NaOH + HCl → NaCl + H₂O
Hier reagieren die Hydroxidionen (OH⁻) der Base mit den Oxoniumionen (H₃O⁺) der Säure zu Wasser. Die übrigen Ionen bilden das Salz Natriumchlorid.
Auch im Alltag spielt Neutralisation eine Rolle. Bei Sodbrennen enthalten viele Antazida basische Stoffe wie Magnesiumhydroxid oder Aluminiumhydroxid, die überschüssige Magensäure neutralisieren und so den pH-Wert regulieren.
Basische Lösungen und Indikatoren
Ob eine Lösung basisch oder sauer ist, kann man mit Indikatoren nachweisen. Diese Stoffe ändern ihre Farbe abhängig vom pH-Wert.
- Lackmuspapier färbt sich in basischer Lösung von rot nach blau.
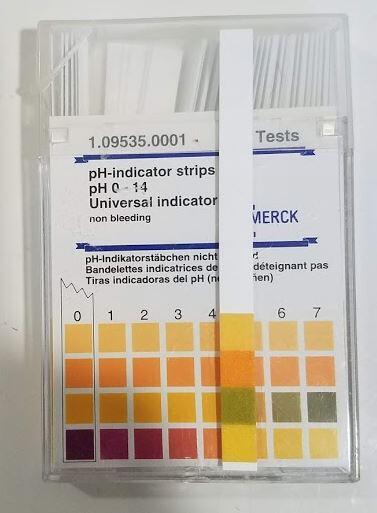
- Ein Universalindikator zeigt je nach pH-Wert verschiedene Farben auf einer Skala von sauer bis stark basisch.
Noch genauer misst ein pH-Meter. Es bestimmt den pH-Wert elektronisch und liefert exakte Zahlenwerte statt Farbschätzungen.
🧪 Schutz tragen:
Schutzbrille immer aufsetzen
Bei Bedarf Handschuhe tragen
Spritzer vermeiden
🚫 Nie probieren oder anfassen:
Chemikalien niemals kosten
Hautkontakt vermeiden – auch bei „milden“ Laugen
💦 Bei Kontakt sofort handeln:
Haut oder Augen mehrere Minuten mit viel Wasser spülen
Sofort Lehrkraft oder Aufsicht informieren
⚡ Wichtig zu wissen:
Auch Laugen können stark ätzend sein
„Verdünnt“ heißt nicht automatisch „ungefährlich“
In der analytischen Chemie nutzt man diese Prinzipien auch bei der Titration: Dabei wird eine Säure oder Base mit einer Maßlösung bekannter Konzentration versetzt, bis der Neutralpunkt erreicht ist. Ein Indikator zeigt den Umschlagspunkt an.
Verseifung
Basen reagieren mit Fetten in einer sogenannten Verseifungsreaktion. Dabei entstehen Fettsäuresalze – also Seifen – und Glycerin. Genau deshalb fühlen sich basische Lösungen oft glatt oder „seifig“ an.
Allerdings bedeutet dieses Gefühl nicht, dass die Lösung sanft ist. Im Gegenteil: Die Base greift dabei die natürlichen Fette der Haut an. Deshalb können starke Laugen die Haut austrocknen oder schädigen.
Ätzwirkung und Konzentration
Die ätzende Wirkung vieler Basen beruht auf den Hydroxidionen (OH⁻). Sie reagieren mit Bestandteilen von Zellen, insbesondere mit Proteinen und Fetten, und zerstören deren Struktur.
Dabei ist wichtig zu unterscheiden: „Stark“ und „konzentriert“ sind nicht dasselbe.
Eine starke Base dissoziiert weitgehend in Ionen. Eine konzentrierte Lösung enthält viele Teilchen pro Volumen.
Eine verdünnte Lauge enthält weniger OH⁻-Ionen pro Liter und wirkt deshalb meist weniger aggressiv als eine hochkonzentrierte Lösung. Dennoch sollte man auch mit verdünnten Basen vorsichtig umgehen.
Anwendungen von Basen
Basen sind überall von Küche bis Industrie. Sie spielen eine wichtige Rolle im Alltag, im menschlichen Körper und in zahlreichen technischen Prozessen. Wir zeigen dir einige typische Beispiele und erklären kurz, warum Basen dort eingesetzt werden:
| Base / Stoff | Anwendung | Chemischer Hintergrund |
|---|---|---|
| Natron (NaHCO₃) / Backpulver | Backen (Teig lockern) | Reagiert mit Säuren. Reaktion: CO₂ entsteht, der Teig geht auf |
| Natriumhydroxid (NaOH) | Abflussreiniger | Löst Fette durch Verseifung, zersetzt organisches Material |
| Seifen / Waschmittel (basisch) | Reinigung von Fett & Schmutz | Basen spalten Fette. Es bilden sich wasserlöslicher Fettsalze |
| Hydrogencarbonat (HCO₃⁻) | Säure-Basen-Haushalt im Blut | Puffersystem hält den Blut-pH stabil (ca. 7,4) |
| Carbonate (z. B. CaCO₃) | Bodenkalkung | Neutralisieren saure Böden und verbessern Wachstumsbedingungen |
| Natriumhydroxid (NaOH) | Papierherstellung, Seifenproduktion, Chemieindustrie | Stark basisch, spaltet organische Stoffe, vielseitig einsetzbar |
| Calciumhydroxid (Ca(OH)₂) | Bauwesen (Kalkmörtel), Wasseraufbereitung | Neutralisiert Säuren, bindet Schadstoffe |
| Ammoniak (NH₃) | Düngemittelproduktion, chemische Synthesen | Grundlage für Stickstoffverbindungen (z. B. Ammoniumnitrat) |
Klassifikation von Basen
Wie bei Säuren hilft eine Einteilung, den Überblick zu behalten. Basen lassen sich nach ihrer Stärke, ihrem Aufbau und ihrer Reaktionsweise unterscheiden. Diese Einteilungen machen es leichter zu verstehen, warum manche Basen sehr heftig reagieren und andere eher mild wirken.
Starke und schwache Basen
Basen unterscheiden sich vor allem in ihrer Stärke.
Starke Basen bilden in Wasser nahezu vollständig Hydroxidionen (OH⁻). Das Gleichgewicht liegt also fast vollständig auf der Seite der Ionen. Typische Beispiele sind Natriumhydroxid (NaOH) oder Kaliumhydroxid (KOH). Solche Basen erhöhen den pH-Wert stark.
Schwache Basen reagieren dagegen nur teilweise mit Wasser. Es stellt sich ein Gleichgewicht ein, bei dem sowohl unveränderte Moleküle als auch Ionen vorhanden sind. Ein bekanntes Beispiel ist Ammoniak (NH₃).
Die Stärke einer Base beschreibt man mit der Basenkonstante (Kb) oder dem pKb-Wert.3 Ohne ins Zahlenchaos zu geraten, gilt: Je kleiner der pKb-Wert, desto stärker ist die Base.
Hydroxidbasen und Basen ohne OH⁻ im Molekül
Ein weiterer Unterschied liegt im Aufbau der Base.
Manche Basen enthalten das Hydroxidion bereits direkt im Molekül, zum Beispiel NaOH oder KOH. Löst man sie in Wasser, werden die OH⁻-Ionen sofort freigesetzt.

Andere Basen besitzen kein OH⁻-Ion in ihrer Struktur. Ammoniak (NH₃) ist ein typisches Beispiel. Es bildet Hydroxidionen erst durch Reaktion mit Wasser.
Diese Unterscheidung hilft oft mehr als komplizierte Begriffe wie „Metallhydroxide“ oder „Amine“, weil sie direkt zeigt, woher die OH⁻-Ionen stammen.
Einwertige und zweiwertige Basen
Basen kann man außerdem danach einteilen, wie viele Hydroxidionen sie pro Teilchen liefern können.
Einwertige Basen wie NaOH geben pro Molekül ein OH⁻-Ion ab.
Zweiwertige Basen wie Calciumhydroxid (Ca(OH)₂) können zwei OH⁻-Ionen freisetzen.
Praktisch bedeutet das: Zweiwertige Basen können – bei gleicher Stoffmenge – mehr Hydroxidionen liefern und damit einen stärkeren Einfluss auf den pH-Wert haben.
Referenzen
- Brönsted-Lowry-Konzept | LEIFIchemie. (n.d.-a). https://www.leifichemie.de/saeuren-und-basen/saeure-base-theorie-nach-broensted-und-lowry/grundwissen/broensted-lowry-konzept
- Lewis, G. N. (1923). Der Säure-Base-Begriff von Lewis. https://www.chemie-biologie.uni-siegen.de/ac/hjd/lehre/ac1/vortraege0607/hermann_s%C3%A4ure-base-begriff_lewis_corr.pdf
- Mortimer, C. E., & Müller, U. (2010). Chemie: das Basiswissen der Chemie.
Mit KI zusammenfassen:















