Säuren begegnen dir öfter, als du denkst: im Zitronensaft, im Essig, in kohlensäurehaltigen Getränken und sogar im Magen. Hinter dem „sauren“ Geschmack steckt aber vor allem Chemie. Säuren sind chemische Substanzen, die in wässriger Lösung Protonen (H⁺-Ionen) abgeben und dadurch den pH-Wert der Lösung senken.
Säuren sind dabei nicht nur Laborstoffe, sondern echte Alltagshelden. Sie haben spezifische chemische Eigenschaften, die man vom Entkalken im Haushalt über Lebensmittel und Medizin bis hin zur großen Industrie gezielt nutzen kann. In diesem Artikel schauen wir uns Schritt für Schritt an, wie Säuren definiert werden, welche Eigenschaften sie chemisch und physikalisch auszeichnen und welche wichtigen Beispiele und Anwendungen du kennen solltest.

Was sind Säuren? Definition und Grundidee
Um den Begriff wirklich zu verstehen, lohnt sich ein Blick darauf, wie Säuren im Alltag auftreten und wie sie chemisch definiert werden.
Säuren im Alltag
Wenn du in eine Zitrone beißt oder Essig riechst, denkst du sofort an „sauer“. Tatsächlich war der saure Geschmack lange Zeit das wichtigste Erkennungsmerkmal für Säuren. Doch: „sauer“ schmecken ist keine chemische Definition, sondern nur eine Beobachtung. Nicht jede saure Substanz sollte probiert werden, denn viele sind stark ätzend oder gesundheitsschädlich.
Hier stellen wir dir einmal einige wichtige Säuren und ihre Anwendungen vor:
| Name der Säure | Strukturformel / Summenformel | Typische Einsatzgebiete |
|---|---|---|
| Salzsäure | HCl | Magensäure im Körper, Metallreinigung, chemische Industrie |
| Schwefelsäure | H2SO4 | Herstellung von Düngemitteln, Autobatterien, chemische Grundindustrie |
| Salpetersäure | HNO3 | Düngemittelproduktion, Herstellung von Kunststoffen und Farbstoffen |
| Phosphorsäure | H3PO4 | Lebensmittelzusatz (z. B. Cola), Rostumwandler, Düngemittel |
| Essigsäure | CH3COOH | Essig, Lebensmittelkonservierung, Haushaltsreiniger |
| Zitronensäure | C6H8O7 | Entkalker, Lebensmittelzusatz, Geschmacksstoff |
| Kohlensäure | H2CO3 | Kohlensäurehaltige Getränke, Bestandteil des CO2-Kreislaufs |
| Flusssäure | HF | Glasätzen, Halbleiter- und Chipindustrie (sehr gefährlich) |
| Ameisensäure | HCOOH | Konservierung, Leder- und Textilverarbeitung |
| Ascorbinsäure | C6H8O6 | Vitamin C, Antioxidationsmittel in Lebensmitteln |
Außerdem sind Säuren nicht immer flüssig. Ein typisches Beispiel ist Zitronensäure, die als weißer, kristalliner Feststoff vorkommt. Auch Vitamin C (Ascorbinsäure) ist fest. Entscheidend ist also nicht der Aggregatzustand, sondern das chemische Verhalten der Substanz.
Die wichtigste Definition (Brønsted)
In der modernen Chemie verwendet man meist die Definition nach Brønsted und Lowry.1 Danach ist eine Säure ein Protonendonator, also ein Stoff, der ein Proton (H⁺) abgeben kann. Eine Base ist entsprechend ein Protonenakzeptor und nimmt ein Proton auf.
Reagiert eine Säure mit Wasser, überträgt sie ein Proton auf ein Wassermolekül. Dabei entsteht ein sogenanntes Oxoniumion (H₃O⁺). Genau diese Ionen sind für die typischen Eigenschaften saurer Lösungen verantwortlich.
Säuren in Wasser: pH-Wert als Messgröße
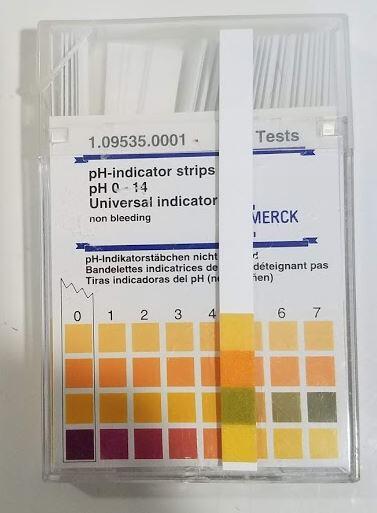
Ob eine Lösung sauer ist, erkennt man am pH-Wert. Liegt dieser unter 7, spricht man von einer sauren Lösung. Je kleiner der pH-Wert, desto höher ist die Konzentration an H₃O⁺-Ionen.
Der pH-Wert gibt also an, wie viele Oxoniumionen in einer Lösung vorhanden sind und damit, wie stark die saure Wirkung ist.
Klassifikation von Säuren
Säuren lassen sich auf unterschiedliche Weise einteilen. Diese Klassifikationen helfen dir, Ordnung in die vielen verschiedenen Stoffe zu bringen, die in der Chemie als Säuren bezeichnet werden.
Starke und schwache Säuren

Ein wichtiges Unterscheidungsmerkmal ist die Säurestärke. Starke Säuren geben in Wasser (nahezu) alle ihre Protonen ab.2 Man sagt, sie dissoziieren fast vollständig. Ein typisches Beispiel ist Salzsäure (HCl). In wässriger Lösung liegen fast nur noch H₃O⁺-Ionen und Chlorid-Ionen vor.
Schwache Säuren dagegen geben ihre Protonen nur teilweise ab. Es stellt sich ein Gleichgewicht ein: Ein Teil der Moleküle bleibt „ganz“, ein anderer Teil reagiert mit Wasser. Essigsäure ist ein klassisches Beispiel für eine schwache Säure.
Die Stärke einer Säure wird mit dem pKs-Wert (oder pKa-Wert) beschrieben. Je kleiner dieser Wert ist, desto stärker ist die Säure.
Einprotonige und mehrprotonige Säuren
Säuren unterscheiden sich auch darin, wie viele Protonen sie abgeben können. Einprotonige (monoprotische) Säuren wie HCl geben ein Proton ab. Zweiprotonige (diprotische) Säuren wie Schwefelsäure (H₂SO₄) können zwei Protonen abgeben, dreiprotonige (triprotische) wie Phosphorsäure (H₃PO₄) sogar drei.
Dabei gilt meist: Das erste Proton wird am leichtesten abgegeben. Jedes weitere Proton „sitzt“ stärker gebunden und geht schwerer in Lösung.
Organische und anorganische Säuren
Neben der Einteilung nach Stärke oder Protonenzahl unterscheidet man auch zwischen organischen und anorganischen Säuren. Der Unterschied hängt vor allem mit ihrem chemischen Aufbau zusammen.
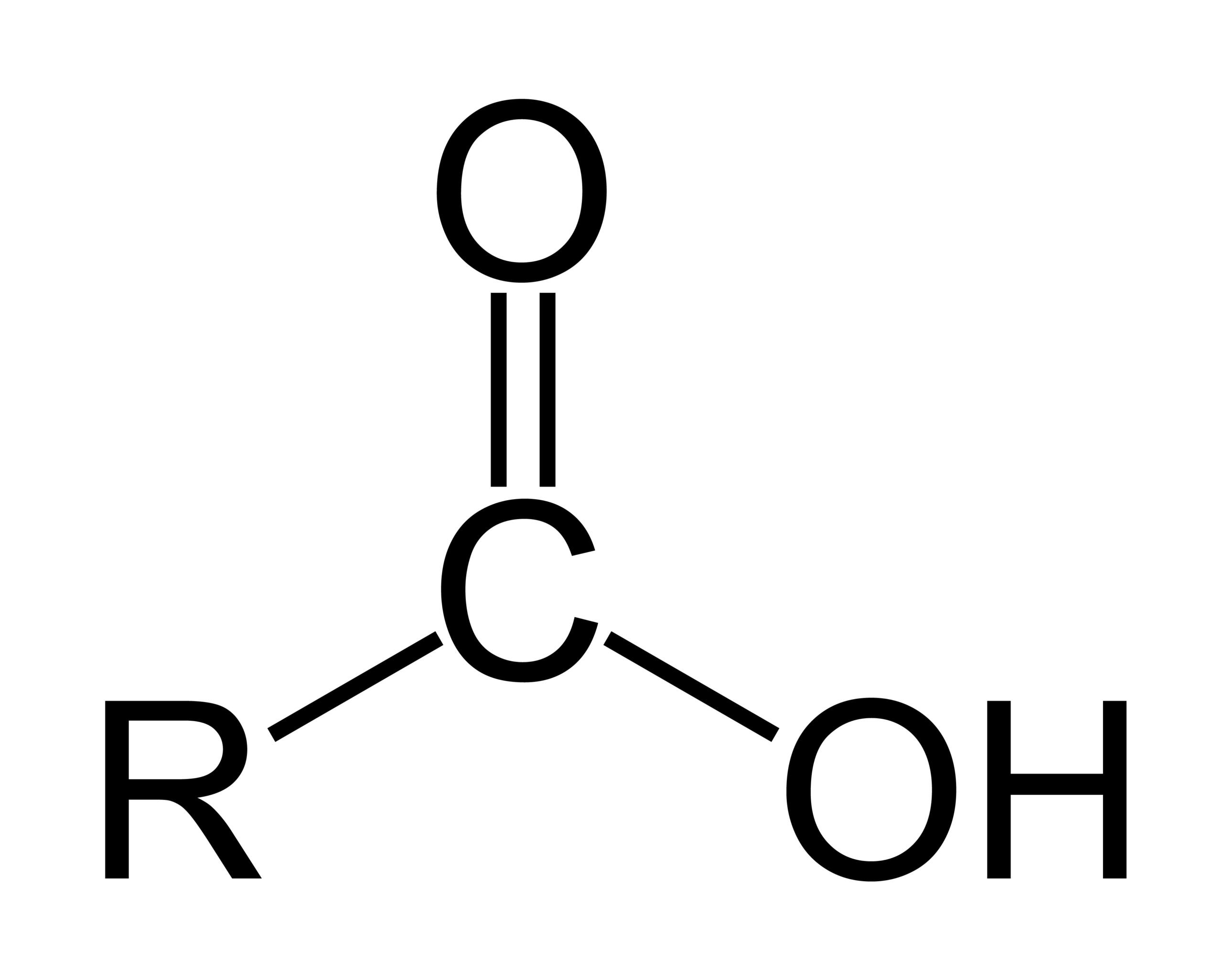
Organische Säuren gehören zur organischen Chemie und enthalten Kohlenstoff als zentrales Element. Meist besitzen sie eine sogenannte Carboxylgruppe (-COOH), die für ihre sauren Eigenschaften verantwortlich ist.
Typische Beispiele sind Essigsäure (CH₃COOH), Zitronensäure oder Ameisensäure. Viele organische Säuren kommen in Lebensmitteln oder in der Natur vor.
Anorganische Säuren (oft auch Mineralsäuren genannt) gehören zur anorganischen Chemie. Sie bestehen meist aus Wasserstoff und einem Nichtmetall wie Chlor, Schwefel oder Stickstoff. Beispiele sind Salzsäure (HCl), Schwefelsäure (H₂SO₄) oder Salpetersäure (HNO₃). Diese Säuren spielen eine große Rolle in Industrie und Technik und sind häufig stärker als organische Säuren.

Chemische Eigenschaften von Säuren
Die chemischen Eigenschaften von Säuren zeigen sich vor allem in typischen Reaktionen, die im Unterricht immer wieder vorkommen. Viele dieser Reaktionen lassen sich auf die Abgabe von Protonen (H⁺) bzw. die Bildung von Oxoniumionen (H₃O⁺) zurückführen.
Protolyse und Säure-Base-Reaktion
Die grundlegende Reaktion einer Säure ist die sogenannte Protolyse. Das ist die Übertragung eines Protons auf einen Reaktionspartner.3 Trifft eine Säure auf eine Base, spricht man von einer Säure-Base-Reaktion oder Neutralisation.

Dabei entsteht als Grundprinzip:
Säure + Base → Salz + Wasser
Ein klassisches Beispiel ist die Reaktion von Salzsäure (HCl) mit Natronlauge (NaOH):
HCl + NaOH → NaCl + H₂O
Hier gibt die Säure ein Proton ab, die Base nimmt es auf. Am Ende entstehen Kochsalz (NaCl) und Wasser. Im Alltag begegnet dir dieses Prinzip zum Beispiel bei Antazida gegen Sodbrennen. Sie enthalten basische Stoffe, die überschüssige Magensäure neutralisieren.
Weißt du, was der Unterschied zwischen einer Base und einer Lauge ist?
Reaktion mit Metallen
Säuren reagieren außerdem mit vielen unedlen Metallen. Dabei entsteht ein Salz und das Gas Wasserstoff (H₂).
Ein typisches Beispiel ist Magnesium:
Mg + 2HCl → MgCl₂ + H₂
Das Metall gibt Elektronen ab, während die Protonen der Säure zu Wasserstoffgas reagieren. Dabei bilden sich oft sichtbare Gasbläschen. Wichtig ist: Nicht alle Metalle reagieren gleich stark. Edelmetalle wie Gold oder Platin reagieren mit gewöhnlichen Säuren kaum oder gar nicht.
Reaktion mit Carbonate
Auch die Reaktion von Säuren mit Carbonaten, also kalkhaltigen Stoffen wie Calciumcarbonat (CaCO₃) ist besonders bekannt. Dabei entsteht Kohlenstoffdioxid (CO₂), das als Gas entweicht und es bilden sich Bläschen.
CaCO₃ + 2HCl → CaCl₂ + CO₂ + H₂O
Diese Reaktion kennst du vom Entkalken eines Wasserkochers oder von Kalkflecken im Bad. Säuren lösen Kalk, weshalb Naturstein wie Marmor empfindlich auf saure Reiniger reagiert.
Indikatoren und Nachweis von Säuren
Ob eine Lösung sauer ist, erkennt man nicht am Geschmack, sondern mit geeigneten Nachweismethoden. Eine einfache Möglichkeit sind sogenannte Indikatoren. Das sind spezielle Farbstoffe, die ihre Farbe je nach pH-Wert verändern.
Säuren können – je nach Art und Konzentration – ätzend oder gesundheitsschädlich sein. Deshalb gelten im Labor und im Unterricht klare Sicherheitsregeln:
🧪 Schutzausrüstung tragen
Immer Schutzbrille 👓, Laborkittel 🥼 und ggf. Handschuhe 🧤 verwenden. Spritzer können Augen und Haut schwer schädigen.
🔥 Vorsicht beim Verdünnen
Beim Mischen entsteht Wärme. Deshalb gilt:
Erst das Wasser, dann die Säure, sonst geschieht das Ungeheure!
🚫 Nicht probieren oder direkt riechen
Säuren dürfen niemals gekostet werden. Gerüche prüft man – wenn überhaupt – nur vorsichtig durch „Heranwinken“ mit der Hand.
🧴 Bei Kontakt sofort handeln
Kommt Säure auf die Haut, sofort mit viel Wasser spülen und die Lehrkraft informieren. Bei Augenkontakt: sofort zur Augendusche!
🏷️ Gefäße beschriften und vorsichtig arbeiten
Säuren immer eindeutig kennzeichnen und nie in andere Behälter umfüllen, ohne sie korrekt zu beschriften.
Ein klassisches Beispiel ist Lackmus: In saurer Lösung färbt sich blaues Lackmuspapier rot. In basischer Lösung passiert das Gegenteil. Noch genauer arbeitet ein Universalindikator oder pH-Papier. Hier zeigt eine Farbskala an, in welchem pH-Bereich sich die Lösung befindet – von rot (stark sauer) über grün (neutral) bis blau-violett (basisch).
Chemisch betrachtet sind Indikatoren selbst schwache Säuren oder Basen. Ihre Moleküle können in zwei verschiedenen Formen vorliegen – einer „sauren“ und einer „basischen“.
Diese beiden Formen haben unterschiedliche Farben. Je nach Konzentration der H₃O⁺-Ionen verschiebt sich das Gleichgewicht zwischen diesen Formen und damit auch die sichtbare Farbe.
Für eine besonders genaue Messung verwendet man ein pH-Meter. Dieses elektronische Messgerät bestimmt den pH-Wert über eine spezielle Glaselektrode.
Es misst die Spannung, die durch die H₃O⁺-Ionen in der Lösung entsteht, und berechnet daraus den exakten pH-Wert. Während Indikatorpapier nur einen ungefähren Bereich anzeigt, liefert das pH-Meter sehr präzise Werte mit mehreren Dezimalstellen.
Titration: Säuren genau bestimmen
Indikatoren oder pH-Meter spielen auch eine wichtige Rolle bei der Titration. Dabei handelt es sich um ein Verfahren, mit dem man die Konzentration einer Säure oder Base exakt bestimmen kann.

Hat man zum Beispiel eine Säure unbekannter Konzentration, gibt man schrittweise eine Base bekannter Konzentration hinzu. Währenddessen beobachtet man den Farbumschlag eines Indikators oder misst kontinuierlich den pH-Wert mit einem pH-Meter. Sobald die Säure vollständig neutralisiert ist, erreicht man den sogenannten Äquivalenzpunkt.
Aus dem verbrauchten Volumen der Base lässt sich dann berechnen, wie konzentriert die ursprüngliche Säure war.
Mehr über Säure-Base-Reaktionen kannst du auch bei uns lernen.
Physikalische Eigenschaften von Säuren
Neben ihren chemischen Reaktionen besitzen Säuren auch physikalische Eigenschaften, die man beobachten oder messen kann. Dazu gehören Leitfähigkeit, Aggregatzustand, Konzentration und ihr Verhalten beim Verdünnen.
Leitfähigkeit, Konzentration und „Ätzendheit“
Wässrige Säuren enthalten frei bewegliche Ionen wie H₃O⁺-Ionen und negativ geladene Säurerest-Ionen. Diese geladenen Teilchen ermöglichen den elektrischen Stromfluss und deshalb leiten saure Lösungen Strom sehr gut.
Wichtig ist außerdem der Unterschied zwischen „stark“ und „konzentriert“. Eine starke Säure gibt ihre Protonen weitgehend ab, eine schwache nur teilweise. Die Konzentration beschreibt dagegen, wie viel Säure insgesamt in der Lösung enthalten ist. Eine stark konzentrierte Lösung einer schwachen Säure kann also durchaus eine deutliche Wirkung zeigen.
Aggregatzustände und typische Merkmale
Säuren können in verschiedenen Aggregatzuständen vorkommen. Schwefelsäure ist eine viskose Flüssigkeit, Chlorwasserstoff (HCl) ist gasförmig, und Zitronensäure oder Vitamin C liegen als feste Stoffe vor.
Auch Farbe oder Geruch sind kein verlässliches Erkennungsmerkmal: Viele Säuren sind farblos, einige – wie konzentrierte Salzsäure – können jedoch stark riechen oder „rauchend“ erscheinen.
Verdünnen = exotherm
Beim Verdünnen vieler konzentrierter Säuren entsteht Wärme – der Vorgang ist exotherm. Besonders die Bildung und starke Hydratisierung von H₃O⁺-Ionen setzt Energie frei. Diese freiwerdende Energie wird als Wärme spürbar, und die Lösung kann sich stark erhitzen.
Deshalb gilt im Labor die wichtige Regel:
Erst das Wasser, dann die Säure, sonst geschieht das Ungeheure.
Labor-Regel
Gibt man Wasser direkt auf eine konzentrierte Säure, befindet sich nur wenig Flüssigkeit an der Oberfläche. Die entstehende Wärme kann das kleine Wasservolumen schlagartig zum Sieden bringen.
Wird dagegen die Säure langsam in eine größere Menge Wasser eingerührt, verteilt sich die Wärme besser im gesamten Volumen. Die Temperatur steigt kontrollierter an und das Risiko des Verspritzens ist deutlich geringer.
Referenzen
- Brönsted-Lowry-Konzept | LEIFIchemie. (n.d.-b). https://www.leifichemie.de/saeuren-und-basen/saeure-base-theorie-nach-broensted-und-lowry/grundwissen/broensted-lowry-konzept
- Schlederer, M. (2025, December 31). Säurestärke | MEDAT-relevant. MEDBREAKER | MedAT. https://www.medat-vorbereitung.at/der-medat/chemie/saeure-base-reaktionen/saeurestaerke/?srsltid=AfmBOorxKKIU6f3gxxJqxOznI4iOK0x8wdi9jtRS5f2GeI31e9887bvi
- Protolyse. (n.d.). https://www.chemie.de/lexikon/Protolyse.html
Mit KI zusammenfassen:
















